 发病机制
发病机制
发病机制:子宫内膜异位的主要病理变化为异位内膜随卵巢激素的变化发生周期性出血,伴有周围纤维组织增生和粘连形成。子宫内膜异位病变通常为多处,有表浅的,也可有较深的浸润、深部浸润及广泛病变,可引起盆腔器官、腹膜表面及肠管粘连成团。在病变区可见紫褐色斑点或小泡,最终可发展为大小不等的紫蓝色实质结节或包块。子宫内膜异位病灶的外观表现主要取决于病变时间的长短、部位、大小及浸润深度而有所差异。子宫内膜异位症的好发部位(图1)。
1.卵巢子宫内膜异位症 卵巢子宫内膜异位症最为多见,据报道发生于卵巢的子宫内膜异位症为40%~50%,约80%累及一侧卵巢,50%同时涉及双侧卵巢。早期在卵巢表面可见灰红色、棕色、蓝色的病变区。随着病变的发展,异位的内膜向卵巢皮质侵入,异位内膜可因反复出血而形成单个或多个囊肿,但以单个为多见,称为卵巢子宫内膜异位囊肿,囊肿内含有暗褐色糊状陈旧性血液,状似巧克力液体,故又称为卵巢巧克力囊肿。由于这种囊肿在初期常有穿破特点,一般不会长得很大,一般直径多在5~6cm以下,很少超过10cm,但也有直径达25cm左右者,囊肿增大时表面呈灰蓝色,可有棕色斑块镶嵌。经期囊肿内出血增多,囊内压力增高,囊壁可出现小的裂隙,并可有极少量血液渗漏,裂隙随即被漏出物引起的腹膜局部炎性反应和组织纤维化所闭合,造成卵巢与周围组织如子宫、阔韧带或乙状结肠、直肠等紧密粘连,被固定于盆腔内。手术分离过程中囊肿往往破裂,为卵巢子宫内膜异位囊肿的特征之一。
2.子宫后壁下段、宫骶韧带、直肠子宫陷凹、直肠阴道隔的子宫内膜异位症这些部位均于盆腔较低部位,与经血中的子宫内膜碎屑接触机会最多,故为子宫内膜异位症的好发部位。在这些部位病变为蓝色、棕色或黑色结节或纤维化粘连之斑块。当结节或斑块位于宫骶韧带或阴道直肠隔时,即使病变较小仍可触及。随着病变的发展,可累及双侧卵巢,阴道直肠隔,并造成盆腔广泛粘连,使子宫直肠陷凹变浅或消失。宫骶韧带及直肠陷凹部位的病变可发展侵入到直肠与阴道,形成可经阴道检查发现的结节,向阴道后穹隆或直肠突出,累及直肠的肌层,可形成粘连,造成管腔粘连,但极少穿透直肠黏膜层。
3.宫颈、阴道、外阴部的子宫内膜异位症 这些部位的子宫内膜异位症一般较少见,且症状一般不典型。阴道子宫内膜异位症可能由子宫直肠陷凹的病灶蔓延而来。宫颈子宫内膜异位病灶可能由于经前宫颈电灼或激光等手术创面未愈合而月经来潮,由子宫内膜碎屑种植而致,宫颈深部的病灶也可能系直肠子宫陷凹异位灶直接蔓延而来。外阴部的子宫内膜异位症也可由于分娩时将子宫内膜种植于外阴伤口而致。宫颈部位的异位病灶可见宫颈表面暗红或紫蓝色小颗粒;阴道部病灶为紫蓝色硬节或多个息肉样突起;外阴部病灶可于病灶部位触及硬节,并随月经周期而变化,经期增大、胀痛,经后缩小,症状消失。
4.输卵管子宫内膜异位症 一般直接累及输卵管者较少,偶可在其管壁浆膜层见到紫蓝色斑点或小结节,输卵管与周围病变组织粘连,造成输卵管扭曲而影响输卵管的蠕动功能,但输卵管一般通畅。据文献报道输卵管子宫内膜异位症占10%,输卵管系膜子宫内膜异位症占10%。
5.肠道子宫内膜异位症 肠道子宫内膜异位症很少见,可累及阑尾、盲肠及乙状结肠、直肠等。其中阑尾子宫内膜异位症占肠道子宫内膜异位症的17%,盲肠占7%,而结、直肠部位占71%。盆腔子宫内膜异位症同时累及阑尾者约占1%。据国外文献报道在子宫内膜异位症中
直肠子宫内膜异位症占5%~10%,阑尾及其他肠段的子宫内膜异位症占2%~5%。在这些部位的病灶,首先侵犯肠管的浆膜层,继而深入肌层,形成坚硬的结节、瘢痕、粘连,造成肠管变形、狭窄,但一般不侵犯黏膜层,因此肠黏膜完整。
6.泌尿道子宫内膜异位症 泌尿道子宫内膜异位症包括膀胱、输尿管、尿道及肾脏子宫内膜异位症。泌尿道子宫内膜异位症约占所有子宫内膜异位症的1.2%,其中累及膀胱者占84%,输尿管占15%,肾脏及尿道极少。病变累及膀胱三角区,患者可出现尿频、尿急、尿痛,由于不侵犯膀胱黏膜,一般不伴血尿。但如果病灶大,经期由于黏膜充血可有轻微血尿。在膀胱镜下,多数病人可显示黏膜下肿块呈紫蓝色突起,经期紫色加深。子宫内膜异位症侵及输尿管时,如果病灶大可发生输尿管梗阻;如果输尿管周围组织如宫骶韧带、宫旁组织发生子宫内膜异位症时,病变可累及输尿管,可致局部输尿管发生扭曲、狭窄、梗阻等,继而发生输尿管扩张、肾盂积水等。
7.腹壁子宫内膜异位症 一般都出现于手术后的腹壁瘢痕,是手术时子宫内膜直接种植所致。一般发生于手术后数月至数年,在腹壁手术瘢痕的部位出现硬节,月经期发生疼痛,硬节增大。病灶多位于腹直肌鞘前后,常累及腹直肌和腹直肌鞘,病灶如向腹壁皮肤侵犯,可穿破皮肤,月经来潮时可见病灶出血。病灶切面呈灰白色或略带黄色,可见多个含棕色液体的小囊。
8.其他部位的子宫内膜异位症 子宫内膜异位症除可发生于上述部位以外,还可发生于身体的其他部位,如腹股沟、脐、肺、横膈等部位,但临床上极为少见。发生于这些部位的子宫内膜异位灶可发生周期性疼痛,并触及肿块,如果为肺或横膈部位病灶,可通过拍片或者CT等发现。在月经期症状加剧,病灶增大。如果为脐部的内膜异位症,可有脐部疼痛,紫蓝色皮下结节,经期且有血性或棕色液体从脐部流出。如发生于肺部的子宫内膜异位症,可出现周期性
咯血。
镜下检查子宫内膜异位症的典型结构为在病灶中可见到子宫内膜上皮、内膜腺体或腺样结构,内膜间质及出血。病灶较少的区域也能看到较正常的内膜组织,并有含铁血黄素的巨噬细胞。在较晚期的病例中,由于反复出血,上述典型的组织结构可能被破坏而难以发现,而出现临床和镜下病检所见不一致现象,临床表现极典型而内膜异位组织病理特征极少。Vervon等(1986)根据肉眼所见病灶色泽,结合镜检所见及含铁血黄素的多寡,将内膜异位症分成4组:①颜色呈红色或透亮,镜检多见内膜腺体及间质无含铁血黄素或仅少量;②颜色呈红棕色,镜检也多见腺体及间质,含铁血黄素少于25%;③颜色呈深棕色,镜检仅见散在的内膜样细胞,含铁血黄素为25%~50%;④病灶呈黑色,镜检看不到内膜细胞,而含铁血黄素超过50%。异位的子宫内膜在卵巢分泌的激素作用下,也发生周期性改变,但其改变不一定与子宫内膜的变化同步,且往往多为增生期改变,是因为异位内膜周围组织纤维化致血供不足有关。
9.子宫内膜异位症恶性变 异位症病例中恶性变者罕见,恶变率<1%,收集世界文献记载不满100例。恶变较易发生于卵巢巧克力囊肿,通常恶变为腺癌。良性的卵巢巧克力囊肿内壁呈红色或暗棕色不一,根据出血范围和持续时间而定;内壁可能薄而光滑或厚似天鹅绒样,根据纤维组织或功能性子宫内膜多少而定。如在囊腔内发现乳头状或息肉样病变,应考虑可能为恶性,其病理诊断标准为:①卵巢必须是良性子宫内膜异位症的部位。②必须是一真正的腺癌。③必须证实从良性至恶性的移行区存在。
 其他辅助检查
其他辅助检查
其他辅助检查:
1.影像学诊断
(1)超声检查:超声检查通常应用在子宫内膜异位症Ⅲ~Ⅳ期的患者,盆腔内形成了子宫内膜异位囊肿,多见卵巢巧克力囊肿。声像图不易与卵巢肿瘤相区别,需结合临床和其他检查予以鉴别。一般在盆腔内可探及单个或多个囊肿,囊肿直径一般为5~6cm,很少>10cm。由于血液机化和纤维沉积,内膜异位囊壁较厚且粗糙不平,囊肿多与周围组织紧密粘连,特别与子宫粘连较紧。月经期由于囊肿内出血,B超下可稍增大。一般将卵巢子宫内膜异位症的声像图分为4种类型:囊肿型、多囊型、混合型和实体型。
①弥漫型子宫腺肌病声像图:
A.子宫增大:子宫呈均匀性增大,在纵或横切面常显示子宫后壁增厚较前壁明显。子宫大小多为≤3个月妊娠子宫,其三径之和平均>20cm左右多见。子宫表面光滑,形态呈球形多见。人们发现子宫的大小在月经期前后常有变化,即子宫在月经期增大,肌层内的液性小暗区明显。而在月经期后子宫则较经期相对为小。这可能与子宫肌层内的积血小囊中的血液部分被吸收以及月经期后子宫充血被改善有关。
B.内部回声:根据弥漫型子宫腺肌病的病理组织结构的不同,其内部回声有2种:
a.液性小暗区征:由于在弥漫型的子宫肌层内有呈增生期或分泌期反应的异位内膜岛,其异位内膜腺体扩张,腺腔内含有蛋白液体或陈旧积血,以致在子宫肌层内形成散在的小囊腔,并使异位内膜周围的平滑肌细胞和纤维结缔组织呈反应性增生。在这样的病理组织结构之间存在着很强的声阻抗界面。因此在声像图上显示均匀性增大的子宫肌层内有散在分布、形态不规则、大小不等的液性小暗区征。在小暗区的周边可显示分布不均匀的强回声光点。光点与暗区常常相互构成编织状征。
b.强回声区:其病理组织结构特点为子宫肌层内只有间质细胞及呈反应性增生的平滑肌细胞和纤维结缔组织,而无异位内膜腺体成分,两者之间无声阻抗差别界面。因此声像图上显示均匀性增大的子宫肌层内仅见分布尚均匀的强回声光点,常以后壁为明显,而显示不出液性小暗区的声像图,即间质性子宫肌腺病。
②局限型子宫腺肌病的声像图:声像图显示子宫多呈不规则形增大,表面凸凹不平,少数子宫大小正常。在子宫的纵横切面上均可见单个或多个呈实质非均质性光团,其内部回声以强回声光点为主,间有少量的散在分布不均的低回声或液性小暗区。光团常位于子宫后壁及双侧子宫角部,稍突起。亦可突向宫腔,类似黏膜下肌瘤。但无论作哪种切面扫查,均只能显示瘤体一侧突向宫腔,另一例与子宫肌层相连,且与肌层之间的界限不清,亦无瘤蒂。而黏膜下肌瘤常有瘤蒂,且整个呈实质均质性光团(瘤体)位于宫腔内。
局限型子宫腺肌病亦称腺肌瘤,其大小一般<3.0cm,1.0cm多见。少数腺肌瘤可>7.0cm,酷似子宫肌瘤,但无假包膜暗带回声。
③合并子宫肌瘤的声像图:两种类型的子宫腺肌病均可合并子宫肌瘤。其声像图特征为子宫明显增大,呈不规则形多见。在子宫纵、横切面图上均可同时显示出子宫腺肌病和子宫肌瘤的声像图特征,两者在声像图上往往不易鉴别。
④合并盆腔内膜异位症的声像图:在声像图上除了可在子宫切面内显示子宫腺肌病的声像图特征,还可在子宫一侧或双侧附件区或直肠凹显示出囊性包块,即卵巢巧克力囊肿或呈不规则形的低回声小光团(盆腔内膜异位结节)。巧克力囊肿的声像图特征为:A.呈非纯净性的囊性包块,即囊内呈液性暗区间散在分布的强光点回声,强光点多积存在囊底部,如用探头加压振动包块时,可见强光点随之漂动。B.囊肿内壁厚而毛糙。其后方有呈内收状的增强效应。C.囊肿多位于子宫后方,且与子宫粘连。盆腔内膜异位结节常位于子宫直肠凹、骶骨韧带、子宫后壁浆膜面上。在纵、横向扫查子宫时,常可在上述部位显示多个<2.0cm大小,形态不规则的低回声光团。如使用直肠水囊法或阴道探头扫查盆腔时,这种声像图特征则更清楚。
2.子宫输卵管造影(HSG) 子宫内膜异位症的HSG影像图特征:①子宫不规则增大,宫体边缘有小囊状阴影;②子宫内树枝状或火炬状阴影,宫体和宫底的两侧缘有毛刷状改变;③双侧输卵管可受压,也可因粘连而增宽;④造影剂在盆腔内弥散不均匀。
子宫以外的异位灶可根据病变的部位行胸片、直肠镜检查。在可疑有泌尿道异位病变时,可作肾盂造影,分泌性和逆行性造影可诊断梗阻部位;病灶波及膀胱时,可行膀胱镜检。卵巢异位B超可发现巧克力囊肿,但无特征性。病变的活组织检查及用激素试验性治疗对确诊有很大帮助。
3.CT和MRI检查 多数病人的诊断及随访以超声诊断为主,CT扫描多表现为边界、轮廓不清、密度不均匀的病灶,有出血者显示为高密度,局部积液为低密度。
MRI的表现多变,根据所用脉冲序列不同及病灶内成分的不同而不同。完全出血性病灶在T1、T2加权图像上为均一密度的高信号,T2加权图像上信号升高。子宫腺肌瘤往往含有较多的二价铁离子,其顺应磁效应可引起病灶信号的降低,尤其在T2加权图像上更明显,影响诊断的准确性。
MRI对卵巢、直肠阴道间隔、阴道周围、直肠乙状结肠之间的内膜异位灶显示较好,但对腹膜及韧带之异位灶显示欠佳。
利用阴道B超和MRI的T2加权图像测定子宫连接层厚度(JZ)有助于诊断子宫腺肌症。其诊断基础是子宫腺肌症的病理变化为子宫内膜腺体和(或)间质深入子宫内膜与肌层的连接处。MRI测定子宫腺肌症的平均JZ厚度分别为(15.0±4.9)mm,正常为(7.7±3.3)mm。MRI诊断腺肌症JZ厚度最佳阈值为≥12mm,敏感性为93%,特异性为91%,阳性预测值阴道B超为71%,MRI是65%,两者差异无显著性。阴道B超和MRI在诊断子宫腺肌症上具有同样的正确性,但在诊断其他种植病灶上CT和MRI的意义不大。
腹腔镜虽然是诊断子宫内膜异位症的最佳方法,但毕竟是侵入性手术,费用高且受到不能反复检查的限制,而CA125的测定、CT及磁共振为非侵入性检查方法,可反复进行。
4.腹腔镜检 在腹腔镜广泛开展前的年代,异位症的诊断主要依靠病史和病理学检查。其典型症状为进行性继发性痛经(经前1~2天开始,月经来潮后1~2天消失)、不孕、性交不适或疼痛。出现排便疼痛或里急后重、尿频或血尿、经间期痛时,应高度怀疑为异位症。妇科检查时发现子宫后屈固定、子宫骶骨韧带结节状粗厚、子宫直肠陷凹处痛性结节、单侧或双侧卵巢肿大及压痛,则更支持此诊断。
由于异位症的病变范围变异更大,微小病灶不易发现。文献报道,如仅根据临床诊断,误诊率可高达40.7%,漏诊率为17.8%,即使应用B超检查,仍难发现按美国生育协会(AFS)分期的Ⅰ或Ⅱ期病例。腹腔镜可直接观察病灶并做活检,以确定异位症是否存在,尤其对无症状妇女或症状重但病理学检查阴性者能早期诊断。腹腔镜还可准确地测定病变范围,做出统一的分期,并根据分期选择合适的治疗。
(1)腹腔镜检查适应证:
①不孕妇女经筛选检查未发现异常者。
②不孕妇女疑有异位症,卵巢囊肿直径>3~5cm者。
③盆腔疼痛症状明显而原因不明者。
④盆腔疼痛伴卵巢囊肿直径>3~5cm者。
⑤子宫输卵管造影图像异常如遮阳伞、蘑菇样或刺刀样图像者。
(2)腹腔镜施行时间:诊断性腹腔镜在月经周期任何时间皆可施行。如临床怀疑异位症存在,则最好在月经期或月经来潮前天施行,因为此时内膜异位病变更为明显,甚至病灶表面可见活动性出血。此外或可窥见经血逆流和伞端滴血现象,此种表现不但有助于诊断,也可解释为什么有些妇女尽管种植灶小而少,痛经却如此剧烈。
(3)腹腔镜观察程序:应全面观察整个盆腔,在子宫操纵器和钝形粗探条的指引下,顺序暴露盆腔腹膜及脏器,检查每一微小病变不致遗漏。先将子宫向后移动,以利观察子宫、膀胱表面及其陷凹处腹膜、圆韧带,继而将子宫举向前位,并分别转向两侧观察输卵管及卵巢,借助探条抬起卵巢,仔细观察卵巢各面,最后探查子宫直肠陷凹及子宫骶骨韧带处有无病灶。如子宫直肠陷凹积有较多液体,应先吸净,使能看清盆底腹膜及子宫骶骨韧带表面。每例均应常规探查阑尾及结肠,使能正确分期。
肉眼及显微镜观察:
①异位症的好发部位为卵巢、子宫骶韧带、子宫直肠陷凹、卵巢窝、膀胱子宫陷凹和盆腔腹膜。上述部位受累最多的原因,推测是由于经血逆流时,经血中子宫内膜碎屑因重力作用坠入盆腔深处而致。卵巢紧邻输卵管伞卵巢表面凹凸不平及频繁发生的排卵孔创面,更增加了其对异位症的易感性,成为异位症的最常见的部位。
②内膜异位病灶的大小、色泽和形状,外观差异很大。典型病变表现为深紫褐色的色素沉着损害。开始出血时为鲜红色或紫蓝色病灶,被
血红蛋白染色后逐渐变成棕褐色或暗紫色,最后形成白色星状瘢痕。初发时常被描述为“火药灼伤”,病灶直径<2mm,历时长后,病灶如“桑葚样”,单个病灶直径约为2~5mm,有的融合成团块或形成囊肿。此种病变看来局限于表面,实际上病变深度极为不同,因此有些病灶仅见“冰山之顶峰”。
非典型病变多为无色素沉着病损,包括:A.腹膜白色不透明区,有或无增厚。B.腹膜红色火焰状损害,常凸出腹膜表面。C.腹膜表面腺体赘生物。D.圆形的腹膜缺陷,或称腹膜窗,可能为瘢痕和受损腹膜边缘凝集形成。E.卵巢下粘连,在卵巢下面和卵巢窝腹膜之间的病损。上述非典型病变经活检证实为异位症的诊断率为45%~81%(表5)。
显微镜下内膜异位种植物已被扫描电镜证实,但此种损害腹腔镜肉眼观不能看到。Murphy等报道对已知异位症病例的正常腹膜随机做活检,用扫描电镜鉴定,25%证实为内膜异位灶。
由于非典型异位症病变或显微镜下种植物的存在,仅凭肉眼判断腹膜种植物数目及大小不可能反映疾病的严重度。
③卵巢的表浅病灶由于反复的周期性出血,引起炎症反应,使盆腔组织粘连。卵巢易固定于卵巢窝接近卵巢门处。腹腔镜窥见外观正常但有粘连的卵巢,应视为异位症可疑;分开粘连后,如溢出巧克力样液体,即有诊断异位症的价值。
随着病程的发展,卵巢紧密地黏于卵巢窝、阔韧带后叶、盆腔侧壁及盆底。有时外观正常但体积增大的卵巢可在子宫后方与另侧卵巢黏在一起成为吻卵巢。
④卵巢巧克力囊肿的形成也呈进行性。早期病变时,卵巢表面或皮质出现紫蓝色小泡,此后融合成为囊肿,大小不一,直径可达8~10cm或更大,常为双侧性,囊壁薄,尚未形成粘连时呈典型的紫蓝色,称卵巢子宫内膜异位囊肿或卵巢子宫内膜瘤。病变初起时囊肿游离,表面光滑;进行性生长后,与周围组织粘连紧密。术中囊肿破裂或穿刺时,可见稠厚的咖啡色液体如巧克力糖浆,故又称卵巢巧克力囊肿。
⑤盆腔腹膜也是异位症的好发部位,且盆腔病灶常为多处并存。异位症患者的盆腔积液量较正常妇女为多,范围为10~130ml,正常妇女<10ml。经期时多为病灶活动性出血引起的鲜红血液,非经期则为陈旧血,或为含铁血黄素染色腹膜所致的棕黄色沉积。盆腔腹膜除存在上述病灶外,往往在盆腔深部可见假囊肿。这是由于流至盆腔的经血刺激腹膜,引起结缔组织反应而发生包裹所致。
⑥内膜异位病变可直接波及输卵管,或因盆腔组织广泛受累使输卵管粘连,但输卵管本身往往通畅。在严重病例,直肠紧黏于子宫后壁,使子宫直肠陷凹部分或完全闭锁。
5.活检 怀疑内膜异位病变处应做活检,以提供正常的组织学诊断。活检应从安全地区取材,即远离重要脏器和血管,不致并发损伤和出血,子宫直肠陷凹、子宫骶骨韧带和卵巢表面是活检的理想部分。
异位症的病理学诊断主要依据显微镜下四种基本结构,即子宫内膜上皮、腺体(或腺样结构)、间质和出血。已知持续有功能的子宫内膜异位病变具有破坏其镜下特征的倾向,因此,早期病变常显示典型的组织学,而体积大的卵巢巧克力囊肿,镜下可能仅显示充满含铁血黄素的巨噬细胞,伴不等量的纤维结缔组织和炎性细胞。重要的是,子宫内膜间质是发生出血的原因,而非腺体或上皮,故即使只见到间质存在,也足以认为系此病的特征。
由于临床实践中往往不能获取足够的活检材料,且1/3活检标本不能证实典型的组织学特征,仅能在内膜异位病灶中发现红细胞、含铁血黄素或充满含铁血黄素的巨噬细胞等出血证据,此时只能结合临床症状及肉眼所见内膜异位病变特征做出诊断,但应注意排除其他病变存在。
 治疗
治疗
治疗:
1.药物治疗
(1)药物治疗的目的:主要为控制症状和解决生育要求,对非子宫内膜异位症所致的疼痛在不能确诊时,为了排除异位病灶的影响,可以试用药物抑制卵巢功能的方案。前已述及,30%~50%的子宫内膜异位症伴有不孕症,对这一部分病人的治疗目的主要是促进生育能力。一般宜从破坏性最小而有效的方法开始,若持续治疗3~6个周期无效,进一步可考虑较为复杂的治疗方案,IVF-ET等助孕技术可作为最后的选择。
(2)药物治疗的方法:药物治疗包括对症治疗和激素抑制疗法,前者适用于病变局限在Ⅰ~Ⅱ期有慢性盆腔疼痛,无生育要求者,对症治疗可能使病情发展,或导致不孕。使子宫内膜萎缩的激素治疗比使蜕膜化的治疗效果好,且在假孕期间,垂体与卵巢功能的抑制强于假绝经疗法。用药期间月经中期的LH、FSH、P、E2水平均降低,外源性的雌/孕激素和子宫内膜以及异位内膜上相应的受体结合,导致内膜萎缩,水肿和蜕膜化等,继而使病灶发生坏死吸收。
①雌激素/孕激素诱发假孕疗法:
A.口服避孕药。由Kistner于1958年首用,此法系持续服用高剂量的雌/孕激素,使产生一种高激素性的闭经,其所产生的变化与妊娠期相似,故名假孕。各种口服避孕药均可用来诱发假孕,其中以含高效孕激素类制剂效果最好,如炔诺孕酮(左旋18甲基炔诺酮)0.5mg+炔雌醇(乙炔雌二醇)0.05mg等。
用法:每天1片,持续6~9个月,每次突破性出血后增加1片,至闭经为止,有效剂量因人而异。疗效:症状的缓解取决于能否诱发闭经。部分患者在治疗的开始,病灶可扩大,症状加重,以后逐步减轻。此法效果较达那唑(danazol),GnRHa的效果为差。其不良反应和禁忌证与避孕药相同。
B.孕激素:单用人工合成的孕激素,通过抑制垂体促性腺激素的分泌,造成无周期性的低雌激素状态,还可与细胞内的孕酮和雄激素受体结合,直接对异位病灶起抗雌激素作用。人工合成的孕激素与内源性雌激素共同起作用,造成高孕激素性的闭经和蜕膜化,形成假孕。但由于内源性雌激素水平波动,容易发生突破性出血,可加用少量雌激素以形成典型的假孕。此法可用于达那唑(danazol)、GnRHa禁忌者。常用的人工合成孕激素制剂可分为两大类:一为C-2l类孕激素,如甲羟孕酮(MPA)等;一为C-19类孕激素,如孕三烯酮(内美通)等,后者的雄性素作用较强。
用法:醋酸甲羟孕酮 (MPA)40mg/d或炔诺酮(nore-thindrone)30mg/d或
醋酸炔诺酮(norethindrone acetate)15mg/d。晚期无生育要求又有手术禁忌证的患者,可用长效醋酸甲羟孕酮(depot-MPA)100~200mg,每月1次。孕三烯酮(内美通)1.25~2.5mg,每周2次,用6个月。
不良反应:较雌/孕激素联合用药少,醋酸甲羟孕酮(depo-MPA)具有吸收和排泄缓慢的特点,故适用于防止残留病灶的复发。但因药物吸收不稳定可引起不规则出血。亦不适用于在治疗后短期内有生育要求者。孕三烯酮(内美通)的不良反应为体重增加(平均增加2.1kg)、头痛、多汗、多毛和不规则出血,停药后可自然恢复。
②达那唑(danazol):20世纪70年代中期开始用于治疗子宫内膜异位症,至今仍为许多国家首选的药物。它是一种甾体衍化物,结构上类似雄激素,17α-乙炔
睾酮,经肠胃道迅速吸收并迅速代谢,由尿及粪便排泄。口服400mg后2h达到血液最高浓度(200µg/ml),平均半衰期为28h,单次口服400mg后,60h
血浆浓度降至27.5ng/ml。
A.作用机制:
a.可与多种受体结合,因而具有多方面的功能,在周围循环内可与性激素结合球蛋白(SHBG)结合,降低SHBG水平,使游离
睾酮升高。在靶细胞内可与雄激素受体结合,达那唑-激素受体复合物进入细胞核,合成新的蛋白质。
b.取代孕激素和
可的松与皮质类固醇结合球蛋白结合。
c.与细胞内雌激素不发生结合。
d.通过与甾体物质竞争活性酶,抑制肾上腺与卵巢甾体生成酶的作用。
e.在下丘脑-垂体水平,抑制中期FSH,LH峰,降低两者的基础水平,并直接作用于卵巢,抑制卵巢甾体生成能力并降低周围循环中的甾体水平,导致在位和异位内膜萎缩。
f.可直接与子宫内膜的雄激素和孕激素受体结合,抑制内膜细胞的增生。
g. 达那唑的免疫调节作用,体外研究显示达那唑可通过
睾丸素、孕激素和糖皮质激素受体,影响细胞内钙及cAMP/cGMP而发挥作用。经达那唑治疗后,体内自身抗体水平明显下降,同时体内免疫球蛋白IgG,IgM,IgA的含量也下降。近年来研究表明,子宫内膜异位症病人外周血中巨噬细胞能促进自身子宫内膜细胞的增生,在加入达那唑后,细胞增生作用明显受到抑制。
B.用法:月经第1天,达那唑200mg,3~4次/d,或12mg/(kg・d),持续6~9个月。在闭经开始后,可减为600mg/d,用药期间,血清E2水平维持在20~50pg/ml。疗程长短取决于个体的反应和疾病的分期,对仅有腹膜种植而无内膜异位瘤者,一般3~4个月的闭经已足够使病灶完全退化。<3cm的内膜瘤,疗程可延长至6个月,>3cm时,常需6~9个月的疗程,但通常病变不能彻底消失,可用外科手术清除之。
C.效果:治疗效果决定于用药的剂量和血清E2反应的卵巢抑制程度。随着用药后闭经的开始症状即出现好转,疗程结束后约90%症状完全消失,腹腔镜下治愈率为70%~90%。妊娠率在800mg/d时为50%~83%。停药1年的复发率为23%,表明存在有残余病灶,以后每年的复发率为5%~9%。
D.不良反应(表6):
③他莫昔芬(三苯氧胺TAM):是一种非甾体类的雌激素拮抗药。当具有正常卵巢功能的妇女服用他莫昔芬(TAM)时,可与雌激素竞争雌激素受体,降低雌激素的效应,并可刺激孕激素的合成,而起到抗雌激素作用。当卵巢功能低下时,他莫昔芬(TAM)表现为弱雌激素作用。
用法:每次10mg,2~3次/d,连续服用3~6个月。
副作用:为潮热,恶心,呕吐,水肿,阴道炎和抑郁等雄激素反应,但反应比达那唑轻。长期应用可能对子宫内膜起雌激素的刺激作用,而引起子宫内膜增生,甚至子宫内膜恶变等。故应严格选择病例,有高危的对象应选用其他方法。
④孕三烯酮(内美通):又名三烯睾诺酮(R-2323)。为19-去甲睾酮的衍生物,20世纪80年代开始用于治疗子宫内膜异位症。它具有复杂的激素与抗激素的特性,因而也是一种适合治疗子宫内膜异位症的药物。研究表明孕三烯酮(内美通)通过与调节基因表达的特异受体结合而对靶组织起作用,它可抑制垂体FSH与LH的分泌,与孕激素受体有强的结合能力,并能与雄激素受体结合,其雄激素作用与炔诺酮相似。对雌激素受体结合的作用微弱。
用法:月经第1天开始,每次2.5mg,每周口服2次,持续6个月。
效果:A.疼痛消失:在治疗的第1个月,60%妇女疼痛减轻或消失,治疗4个月90%的症状有所改善;B.AFS评分:Mettler报道孕三烯酮(内美通)治疗6个月后AFS评分从治疗前的平均15.5分降至2.0分,表明病情明显缩小;C.妊娠率:治疗后24个月的妊娠率为60%左右,略高于达那唑;D.复发率:12%~17%。
⑤GnRHa:人工合成的GnRHa类似物具有两种特性,即对垂体的GnRH受体有高度的亲和力,并可抵抗内肽酶的降解而延长半衰期,长效制剂可维护4周的有效浓度。在应用的早期,认为此化合物有促进妊娠的作用,故命名为GnRH促效剂,后来明确在用药2周后,可出现短暂的FSH、LH升高,继之急剧下降调节作用。常用的制剂和用法(表7)。
药物的疗效因个体而不同,剂量可有增减,一般而言,由于鼻腔充血喷鼻的吸收常不稳定。疗程以6个月为宜,当出现严重低雌激素状况时,疗程相应缩短。治疗效果与达那唑相近。症状完全缓解率>50%,部分缓解率>90%,病灶缩小及腹腔镜评分减少约50%。
副反应:主要为垂体-卵巢轴功能低下,雌激素水平降低所引起的类似绝经期综合征的表现,如潮热、多汗、血管舒缩不稳定、乳房缩小、阴道干燥为常见的反应,占90%左右,一般不影响继续用药。严重雌激素减少(E2<20pg/ml),可增加骨中钙的吸收而发生骨质疏松症,其严重程度不一致,多于停药后恢复。原有偏头痛和抑郁者不宜应用,以免加重原有症状。用药期宜定期检测E2水平来指导用药剂量,至于E2需到何种水平才能表明用药的最佳剂量,以及临床疗效是否与激素低下的严重程度一致等问题,目前尚不甚清楚。Barbieri报道不同组织的雌激素阈值不一,根据子宫内膜对达那唑的反应,在治疗期间E2浓度以20~60pg/ml为宜。
⑥米非司酮:又名RU-486。为人工合成19-去甲基睾酮的衍生物。米非司酮(RU-486)治疗子宫内膜异位症的作用机制主要是其抗孕激素作用,用药后造成闭经,使病灶萎缩。不良反应轻,疗效好,是一种颇有希望的治疗方法。
用法:50mg/d,连续6个月,在用药的第1个月即闭经,用药期间症状消失,约50%患者雄激素保持在生理水平。国内试用低剂量,10mg/d连续90天,亦获满意疗效。其疗效与达那唑和GnRHa相近。
不良反应:主要为抗皮质激素的反应,其他副作用有恶心,呕吐,头晕和疲倦等。
(3)各种药物的比较:
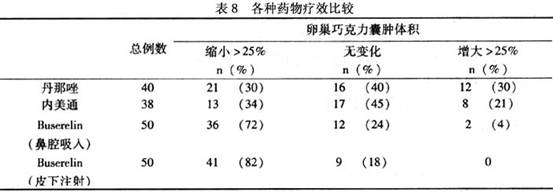
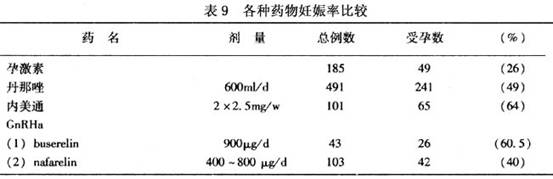
①疗效比较:各药治疗后,绝大多数异位症患者均能消除疼痛,达到很高的症状缓解率,对改善体征则以
布舍瑞林(buserelin)效果最好,其使卵巢巧克力囊肿缩小的疗效显著优于达那唑或孕三烯酮(内美通)(
P<0.01)(表8,9)。AFS评分下降的疗效,仅见于用
布舍瑞林(buserelin)皮下注射治疗重度异位症组,由治疗前(18.5±1.6)分降至治疗后(14.O±2.8)分,差异有极显著意义(
P<0.005)。
②不良反应比较:各种药物的作用机制与其不良反应有关。孕激素类现已少用,国外普遍采用雄激素衍生物或GnRH增效剂。雄激素衍生物的主要不良反应为肝功能损害和雄激素样反应,其中孕三烯酮(内美通)引起的体重增加、皮脂溢、痤疮、多毛显著较达那唑为轻。
GnRH增效剂则仅表现为围绝经期症状。无论何种副反应,停药后均可消失(表10)。
③药物疗效与组织学关系的研究20余年来,治疗异位症的新药相继问世,显示其良好的前景。但不论采用何种药物,总有10%~20%的患者不能获得疗效。其原因归纳有如下几种假说:
A.由于病变周围纤维化,使药物不能到达局部。
B.光镜和电镜证明,异位子宫内膜的形态学和正常子宫内膜不尽相同,病灶处常仅见间质,而无腺上皮。
C.异位内膜细胞可能有其本身的基因程序,而内分泌影响仅是继发的,且因个体细胞分化程度不同,使效应不一。
D.异位内膜中甾体激素受体数目低下。异位内膜不像正常子宫内膜受内分泌调节,从而可能导致其内分泌依附性不足。
药物治疗虽在临床取得良好疗效,但任何一种药物均还存在一个问题,即停药后的复发。为此,Donnez对201例异位症分为5组:达那唑、
利奈孕酮(
炔雌烯醇)、孕三烯酮(内美通)、
布舍瑞林(buserelin)鼻腔吸入和
布舍瑞林(buserelin)皮下注射进行治疗,并有32例对照。治疗6个月后,对卵巢子宫内膜异位残余病灶作组织学检查。结果97%~100%病例切片中,仍能看到子宫内膜腺上皮,其中46%~84%为活动性子官内膜异位症,此与很多文献报告不同。5组中以
布舍瑞林(buserelin)皮下注射治疗后的活动性病变率最低,但均显著高于临床报道的药物治疗后复发率(30%~40%)。
2.手术治疗
(1)开腹手术治疗:外科手术是惟一可以根治本病的手段。由于腹腔镜的普及使用,使得本病得以早期诊断,加上其与不孕的密切关系,因此对年轻而又有生育要求的患者来说,保守性外科治疗越来越显得重要。
保守性手术治疗的目的大致有以下几点:①清除病灶和粘连;②恢复正常解剖关系;③止血;④非创伤性和整形手术。
手术指征:
①疼痛:疼痛指慢性盆腔痛、性交痛和痛经。疼痛的程度与病变的RAFS分级无关,而与病灶的深度和范围相关,故摘除卵巢或抑制卵巢的功能可以治疗疼痛,摘除病灶也可有效的治疗疼痛。
②包块:因卵巢异位囊肿或阔韧带内的异位包块,子宫直肠陷凹内的异位结节和粘连的子宫而行腹腔镜检查,发现其中约0.04%为恶性肿瘤,故应根据患者的年龄、包块大小和性质、患病时间及B超诊断等仔细选择病人。包块大小与性质有关,据报道<5cm者,约1%为恶性;5~10cm者,有11%为恶性;>10cm者,恶性占72%。
③不孕:子宫内膜异位症合并不孕的患者,手术是否为首选治疗意见不一致,如对仅有色素沉着的极早期病变或小的异位灶,手术能否改善受孕率和减轻疼痛,意见不一,反对的意见认为表浅部位的手术非但无效,相反还会造成粘连等不良后果,且显微病灶又无法彻底清除。而主张施行手术治疗的意见则认为子宫内膜异位症患者不孕症的发病率确实高于正常妇女,及时施行腹腔镜检在确诊本病的同时,还可发现其他不孕的原因,并进行必要的治疗,如伴有疼痛者则更应及早进行手术。
剖腹手术操作同常规外科手术。
(2)腹腔镜手术治疗:腹腔镜的优点为方便,恢复快,损伤小且经济。
①表浅异位病灶的处理:小而表浅的病灶可用单极或双极电凝,热凝或气化,尽量将病灶提起,以免损伤周围组织。如能将病灶去除后加凝固效果最好。大的病灶可行钝性分离,继而用剪刀或激光在周围的正常腹膜上进行操作。
②子宫直肠陷凹封闭的处理:子宫直肠陷凹封闭提示有直肠阴道深部的病灶。子宫直肠陷凹部分封闭时,直肠膨起与骶韧带粘连并与子宫相连。部分封闭表示腹膜下有深层种植病灶,使直肠位置改变。当直肠子宫陷凹完全封闭时,常与周围器官粘连。施行手术前应首先明确患者的治疗目的,如为解除疼痛,则应将病灶整块切除。如因不孕,则需以恢复子宫、输卵管和卵巢的解剖和生理功能为主。手术中应仔细辨认邻近器官的解剖,无论用什么种类的手术处理异位病灶,均应从表浅到深层,并尽量将病灶提起,以免损伤邻近器官。最后尽可能地将创面进行腹膜化,预防术后粘连。
③卵巢子宫内膜异位囊肿(巧克力囊肿)手术:卵巢子宫内膜异位囊肿占子宫内膜异位症的50%~70%。其病变表现与其他部位不同,在同一个囊肿内可以表现不同的组织成分,如囊肿上皮、输卵管纤毛上皮、子宫内膜和间质组织,和吞噬有含铁血黄素的巨噬细胞。
A.腹腔镜下卵巢内膜异位囊肿穿刺术:为最简单的手术,适用于小的或粘连紧密不能剥离的囊肿。操作步骤如下:a.于囊肿最突出点进行穿刺;b.吸出囊内液体;c.将囊内和盆腔内冲洗干净;d.电凝或激光破坏囊壁。
B.卵巢异位内膜瘤开窗术:a.于囊肿最突出点行一电凝带,b.沿电凝带作一切口;c.吸除囊内物,冲洗干净;d.电凝切口边缘止血,保留切口开放;e.冲洗。
C.囊壁剥离:a.于囊肿最突出点行一电凝带,沿电凝带作一切口;b.清除囊内容物,边操作边冲洗和吸引;c.分离囊壁与卵巢皮质;d.用抓钳抓住囊壁,顺一个方向扭转;e.囊壁全部扭除后,电凝止血;f.切口保留开放或缝合;g.如囊壁与卵巢不易分离时,找到分界线,用抓钳夹住囊壁提起,看清分界面,用尖头电凝或激光仔细进行分离。
D.卵巢部分切除术:囊肿较大,粘连较紧,不能剥离干净时,可考虑卵巢部分切除术。操作步骤如下a.于囊肿底部与卵巢交界处,电凝或激光切割囊肿;b.尽量保留正常卵巢组织;c.如估计保留的卵巢组织过少,可留下部分囊壁;d.电凝残留囊壁,以防复发;e.缝合卵巢。
E.卵巢摘除术:仅用于卵巢组织已完全被异位内膜组织破坏,且粘连严重无法行卵巢部分切除的情况下。手术操作与其他卵巢囊肿摘除相同;a.抓钳提起卵巢,暴露囊肿蒂部;b.于蒂部结扎3次;c.于第2、3结之间电凝切割下囊肿;d.电凝蒂部止血和防止粘连;e.囊壁可换大号穿刺器取出,必要时可先捣碎后再取出。
3.药物与外科联合治疗 子宫内膜异位症的保守治疗有3种方法:手术,药物抑制和二者合并应用。治疗方式的选择一般取决于疼痛,不孕和病变的严重程度。当前,腹腔镜已在成为所有微小病变,绝大多数轻症病变和多数中到重度病变的首选治疗方法,但大多数学者认为相当一部分患者仍需要合并药物治疗。
外科治疗可恢复正常解剖关系,去除病灶并同时分离粘连,但也有不足之处,如术后的粘连可能导致不孕,严重的粘连使病灶彻底清除,显微镜下和深层的病灶无法看到,术后的并发症有时难以避免等。药物治疗虽有较好的疗效,但停药后短期病变可能复发,致密的粘连妨碍药物到达病灶内而影响疗效。多年来,一直采用手术前后的药物治疗,理想的措施是在用药后的3~6个月无效时,行二次腹腔镜检以明确原因,及时治疗。术后的粘连是影响手术效果的主要原因,术前应用达那唑或GnRHa,在低雌激素的作用下,腹腔内充血减少,毛细血管充血和扩张均不明显,有利于手术的摘除。同时,腹腔液容量减少且清亮,其中纤维蛋白含量降低,使粘连易于剥离,卵巢异位囊肿易于剥离。腹腔内的上述改变,还可以预防术后粘连形成。
术后应用1~2个月的药物,可以抑制手术漏掉的病灶,预防手术后的复发。轻度子宫内膜异位症的病灶清除后,可用不同抑制性药物,因在手术后腹腔内环境改变,有利于生育力的恢复,多数手术后的妊娠发生在手术后的1年以内,在此期间可以考虑诱发排卵治疗,促进生育。手术后6~12个月仍未妊娠,在找出不孕的原因的同时,可给予抑制子宫内膜异位症的药物治疗。
4.治疗方法的选择 子宫内膜异位症的治疗方法很多,主要根据病人的年龄、不孕时间长短、症状严重度、病变范围以及RAFS分期来做出选择。目前认为,病灶的形态学特点和甾体激素受体测定对选择治疗方法将日显重要。
(1)治疗决策前的考虑:
①自然病程:传统观念是随着时间的推移,异位内膜种植物数目及大小进行性增加。Buttram和Betts未能证实病人的年龄和疾病严重程度之间有显著联系,此种间接证据使人推测并非所有异位症病人病情皆有进行性加剧的特点。Thomas和Cooke(1987)报道前瞻性用安慰剂对照研究,在安慰剂应用前后用腹腔镜确定病变范围,结果发现用安慰剂6个月后,病情确有进行性加重;但在17例轻微、轻度异位症中,4例用安慰剂后,病变完全消除。提示轻症病例有可能自然痊愈,但尚需进一步评估确定。如能预测何种病例不治会加剧,何种病例不治可能好转,将对抉择治疗方案有重大价值。
②疾病严重度:首先要考虑的是盆腔器官是否受损和粘连,因为任何一种激素治疗均不能使粘连松解、输卵管复通,即药物对解剖结构变化不可能改善。相反,手术不但能去除内膜异位病灶,且可纠正异位症引起不孕的机械性因素,故是兼治不孕的合理选择。
病变广泛的异位症患者应采取手术治疗,手术方式根据临床分期而定。是否仅用手术一项或与药物联用虽有争论,但大多主张围手术期用药,尤以
布舍瑞林(buserelin)最好。
③年龄与生育状况:病人主诉不孕时,考虑年龄因素尤为重要。对十分年轻的异位症患者,一系列药物治疗是合适的;但对年龄稍大(30岁左右)的妇女,药物治疗可能是浪费时间,此时采取手术治疗更为实际;年龄更大的妇女(40岁以上),如已完成生育,但要求避免卵巢早衰,按
布舍瑞林(buserelin)建议可切除子宫和异位灶,保留全部或部分卵巢组织,以维持内分泌功能。接近绝经期病人(45岁以上),可行药物治疗使能渡过更年期,卵巢功能衰退后异位症常能自愈。但对重度患者或伴有生殖器其他病变时,宜行全子宫及双侧附件切除术。如保留一侧卵巢,可能激活残存的异位内膜而使症状再发,故术后应给予药物治疗3~6个月。
④形态学标准:由于异位内膜的基本组织结构和正常子宫内膜相似,致使人们简单地设想,子宫内膜异位症就是异位的子宫内膜。事实上,异位内膜和自身子宫内膜的形态学、组织化学及生物化学所见常有不同:
A.异位内膜分化程度不一,分化不成熟者对性激素不敏感,尤其对孕激素无反应。因此异位内膜和子宫内膜对内源性卵巢激素的效应可能不同步,而使两者的组织不完全一致。
B.异位内膜代谢功能较差,不论在其腺上皮、表面上皮或螺旋小血管内皮中,碱性磷酸酶活性均较子宫内膜为弱。异位内膜表面上皮及吞噬细胞中酸性磷酸酶活性明显增加,酸性磷酸酶为溶酶体酶,由此提示细胞内分解代谢和自溶作用增强。
C.胞浆和胞核内ER、PR水平及周期性变化也显然有别,异位内膜中ER及PR水平较自身子宫内膜低,且通常只存在一种性激素受体。
利用此种差异可能预测异位症患者对治疗的反应,估计对激素治疗无效应者,应采取手术治疗。
(2)治疗方法的选择:
①期待治疗:对轻微或轻度异位症患者,一些学者建议行期待治疗。Schenken和Malinak报道75%(12/16)轻度异位症未经治疗者,在1年内受孕,而经保守性手术者的妊娠为72.4%(21/25)。Seibel等前瞻性研究结果,19例轻微异位症中,13例在观察1年内受孕,妊娠率为68%;与此相比,13例用达那唑治疗6个月再观察半年者,仅5例受孕,妊娠率为38%。目前认为如患者年轻,病变轻微,经腹腔镜诊断后,可观察等待6~9个月,因30%~60%此种患者虽未治疗也可受孕。
②药物治疗:现已有多种药物可供应用,根据年龄、孕育史及病情轻重做出选择。今后如能用形态学标准来决定治疗方式,将比现在采取的其他标准更起主导作用,有望于达到合适治疗、提高疗效的目的。
③手术治疗:自从新技术的推广应用,包括显微外科技术、腹腔镜和激光手术,使手术治疗地位日显重要。
不孕是异位症的主要症状之一,生育力的恢复是评估疗效的重要标志。Olive和Martin复习文献,对异位症病人采用各种方法治疗后的生育率进行比较,结果为:A.轻度异位症的治疗不能证明何种方法最优越。B.重度异位症以无损伤性显微手术和腹腔镜激光术成功率最高。C.期待疗法和药物治疗的累积妊娠率(生命表法)因分期期别显然不同,期别晚者妊娠率低;而显微手术或腹腔镜激光术后妊娠率与期别无明显关系。
④个体化治疗:异位症患者个体化治疗是最合理的方法。
A.异位症伴不孕:
a.不孕症伴轻微或轻度异位症,如患者年轻、无症状、病变轻可试行期待疗法,但应充分估价其他不孕因素并纠正之。如仍未妊娠,采用经验治疗即药物治疗或保留功能性手术。年龄较大者,期待疗法或长期激素治疗不合适,保守性手术为首选。如以上方法失败,可辅加促进生育措施,根据情况采用子宫直肠陷凹受精、配子输卵管内移植(GIFT)或体外受精(IVF)。
b.不孕症伴中或重度异位症,因存在盆腔粘连,治疗方法与上不同。联合治疗应用最广泛,但年龄较大病人需及早手术,只能考虑短期的围手术期药物治疗。术后受孕失败时,辅助生育措施是进一步的可能选择,根据病变及具体条件决定方法,多半需作IVF。
B.异位症伴盆腔疼痛:
a.要求生育患者:轻微或轻度病变时,参考年龄因素可选用药物治疗或保守性手术。较严重病变妇女则最好采用联合治疗,必要时作骶前神经切除术,以解除盆腔疼痛。
b.无生育要求患者:轻度患者可用非激素药物,目的仅为止痛,也可以应用激素治疗。较严重病变妇女常需联合治疗,因为单用激素症状不易完全缓解。根治性手术通常作为二线治疗,如异位症病程已被药物控制,则保留卵巢功能更为可能(表11)。
⑤复发病例的治疗:治疗后1年内复发率各家报道不一,为16%~52%。复发病例的治疗和初治病例一样,仍是根据病人的症状以决定治疗原则。药物治疗可以控制疾病的发展,同时可用重建手术去除残余病变和纠正解剖学异常。



 流行病学
流行病学
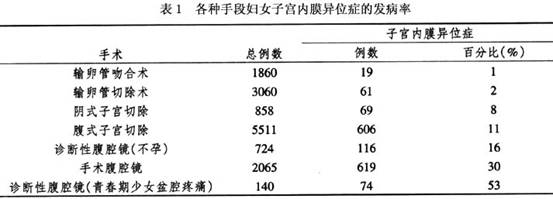
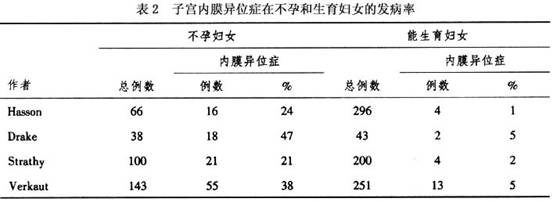

 病因
病因
 发病机制
发病机制

 临床表现
临床表现
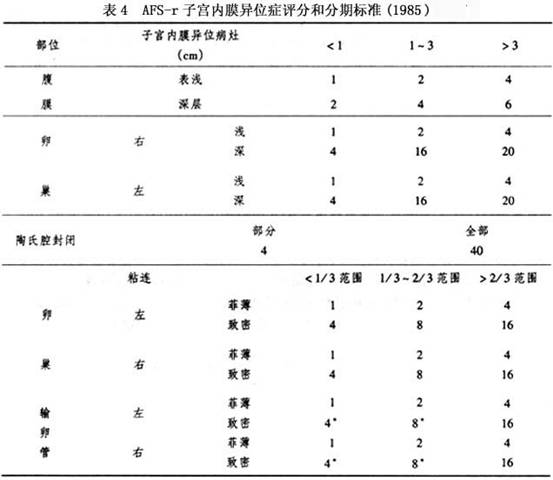
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查

 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗




 预后
预后
 预防
预防